干细胞质量管理规范:确保前沿医学的安全与疗效基石
干细胞技术作为再生医学的核心,正以前所未有的速度改变着疾病治疗的格局。然而,这份蕴含无限生机的潜力,其价值的真正释放,高度依赖于一套严谨、全面且可执行的质量管理规范。这不仅关乎疗效,更是患者安全与行业健康发展的生命线。
为何质量管理是干细胞领域的“高压线”?
干细胞的独特性和多样性决定了其质量管理远比传统药物复杂。从供者筛查、细胞采集、体外培养、诱导分化到最终回输人体,每一个环节都可能引入风险变量。国际细胞治疗协会等权威机构明确指出,质量源于设计,必须将质量控制贯穿于整个细胞“生命历程”。任何细微的偏差,都可能导致治疗失效,甚至引发严重的安全事件。因此,建立并遵循一套标准化、规范化的质量管理体系,是确保干细胞产品安全性、有效性和一致性的根本保障。
核心框架:构建全方位的质量壁垒
一套成熟的干细胞质量管理规范,通常围绕以下几个核心支柱构建:
起始材料与供者管理 质量控制的源头始于供者。严格的健康筛查和知情同意是第一步,确保细胞来源安全、合规且可追溯。对起始生物材料(如脐带血、脂肪组织等)的采集、运输和保存条件必须有明确的标准操作规程,以维持细胞活性与功能。
生产过程控制与标准化 干细胞体外扩增和分化是生产的核心。必须在符合GMP标准的环境中操作,对培养基、血清、生长因子等所有原材料进行严格质控。关键工艺参数,如培养温度、湿度、二氧化碳浓度以及细胞传代次数等,都需要实时监控和记录,确保每一批次产品的一致性与稳定性。
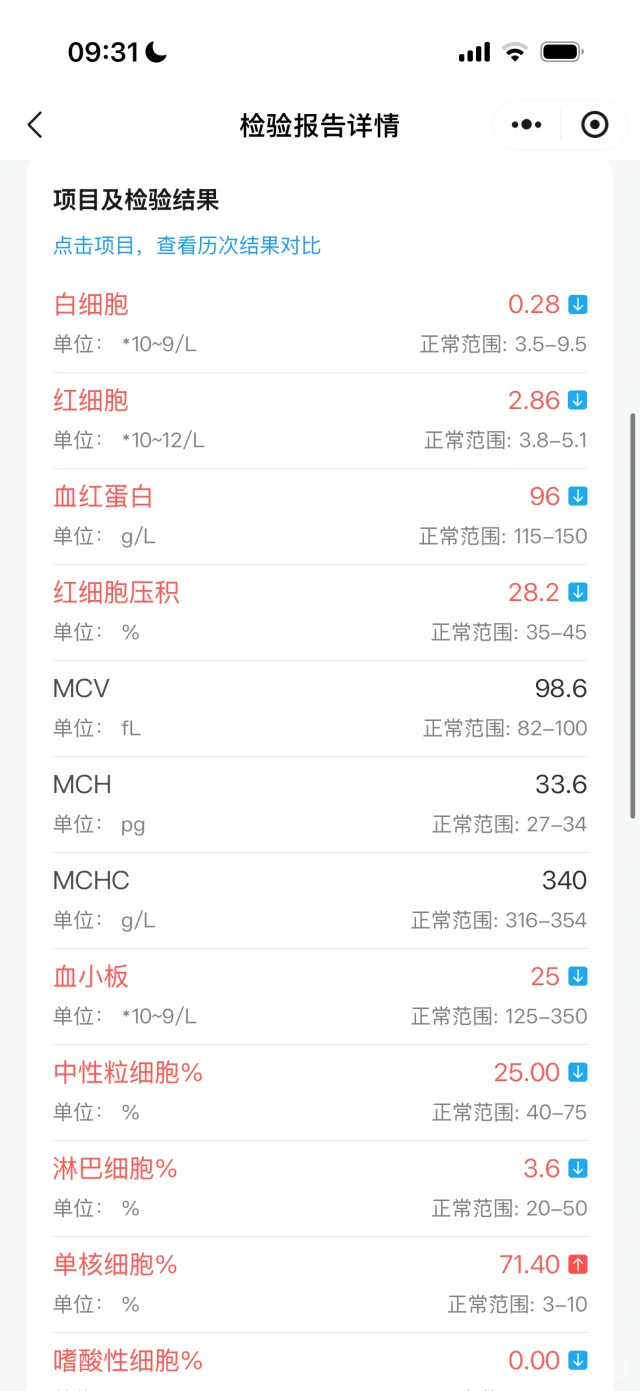
全面的质量检验与放行 干细胞产品在放行前,必须通过一系列严格的检验。这包括但不限于:细胞活性与纯度分析、无菌检查(确保无细菌、真菌、支原体污染)、内毒素检测、身份鉴定(核型分析、STR分型等)以及功能性测定。只有所有指标均符合预设标准的产品,才能用于临床。
可追溯性与文档记录 完整的可追溯体系是质量管理的“铁证”。从供者到受者,所有操作、检验结果、设备校验、人员培训等都必须有清晰、准确、及时的文档记录。这不仅便于问题排查与召回,也是监管审查和持续改进的重要依据。
案例分析:从理念到实践的跨越
以某领先的干细胞库为例,其成功运营的关键在于将质量管理规范深度内化。他们建立了独立的质量保证部门,直接对最高管理者负责,确保了质量监管的独立性和权威性。在细胞制备过程中,他们引入了过程分析技术,对关键质量属性进行实时监控,而非仅仅依赖终产品放行检验,实现了从“事后检验”到“事前预防”的转变。这种前瞻性的管理策略,显著提升了细胞产品的成功率与安全性,为行业树立了标杆。
展望:持续改进与未来挑战
干细胞质量管理规范并非一成不变。随着对干细胞生物学认知的加深和新技术(如基因编辑、3D生物打印等)的涌现,质量管理体系也需动态演进与持续改进。未来,挑战将集中于如何为“个体化”定制细胞治疗建立高效且经济的质控策略,以及如何利用大数据和人工智能来优化质量风险管理。
干细胞质量管理规范是连接前沿科学研究与安全有效临床应用的桥梁。它既是约束,更是保障,是推动整个行业行稳致远的坚实基石。